آشنایی با مفهوم ماده، روشهای طبقهبندی ماده و همچنین روشهای جداسازی مخلوطها از جمله ابتدایی مفاهیمی هستند که در دوران تحصیل به آن پرداخته میشود. شما در زندگی روزمره خود با انواع اقسام مخلوطها سروکار دارید و اگر به صورت تخصصی تر در زمینه شیمی و یا رشتههای مرتبط نیز مشغول به فعالیت باشید، به احتمال زیاد با انواع و اقسام مخلوطها در ارتباط هستید و در برخی موارد لازم است که مخلوطها را از هم جدا کنید. در ادامه، علاوه بر این ابتدا با مفاهیم ماده و روشهای طبقهبندی آن آشنا شده و سپس آموزش عملی متدوالترین روشهای جداسازی مخلوطها را مشاهده خواهید کرد.
ماده چیست؟
به هر چیزی که فضا را اشغال می کند و جرم دارد، ماده گفته میشود. میز و صندلی شما و حتی بدن شما همه از ماده تشکیل شدهاند. هوای اطراف شما هم ماده است که هم فضا را اشغال میکند و جرم دارد. همچنین ما یک نمونه خاص از ماده ، مانند هوا، آب یا شن را یک جسم مینامیم.

روشهای دسته بندی مواد
ما ماده را بر اساس حالت آن (فرم فیزیکی) و ترکیب آن (اجزای اصلی که آن را تشکیل میدهند) دستهبندی میکنیم.
دسته بندی مواد بر اساس حالت فیزیکی
ماده به صورت سه حالت مختلف جامد، مایع و گاز وجود دارد.

ماده جامد
در ماده جامد، اتمها یا مولکولها به یکدیگر نزدیک هستند و در مکانهای ثابت قرار میگیرند. اگرچه اتمها و مولکولها در یک ماده جامد ارتعاش میکنند، اما از روی یکدیگر عبور نمیکنند و به اطراف نیز منتقل نمیشوند. یک جامد دارای حجم ثابت و شکل سخت است. یخ، آلومینیوم و الماس نمونههایی از جامدات هستند.
ماده جامد ممکن است بلوری باشد و اتمها یا مولکولها در الگوهایی با نظم تکراری قرار داشته باشند، یا ممکن است به صورت آمورف باشد و اتمها یا مولکولها هیچ نظمی در نحوه قرارگیری در کنار هم نداشته باشند. نمونههایی از جامدات بلوری شامل نمک و الماس هستند که نظم ساختار بلوری به وضوح در اشکال هندسی آنها مشخص است (اگرچه این مورد برای همه جامدهای بلوری صدق نمیکند). نمونههایی از جامدات آمورف شیشه و پلاستیک هستند.
ماده مایع
در ماده مایع، اتمها یا مولکولها تقریبا به هم نزدیک هستند و به صورت آزادانه نسبت بهم حرکت میکنند، که این امر باعث میشود مایعات حجم ثابتی داشته باشند اما شکل ثابتی نداشته باشند. مایعات شکل ظرفهای خود را به خود میگیرند. آب، الکل و بنزین از جمله موادی هستند که در دمای اتاق به صورت مایع هستند.
ماده گاز
در ماده گازی، اتمها یا مولکولها فاصله زیادی از یکدیگر دارند و آزادانه نسبت به یکدیگر حرکت کنند، که این امر باعث فشردهپذیری گازها میشود. وقتی شما یک بادکنک فشار میدهید یا روی یک تشک هوایی مینشینید، اتمها و مولکولها را به یک فضای کوچکتر میفشارید تا نزدیکتر به هم قرار بگیرند. گازها همیشه شکل و حجم ظرفهای خود را به خود میگیرند. موادی که در دمای اتاق به صورت گازی هستند شامل هلیوم، نیتروژن (اصلیترین مولفه هوا) و دیاکسید کربن میشوند.
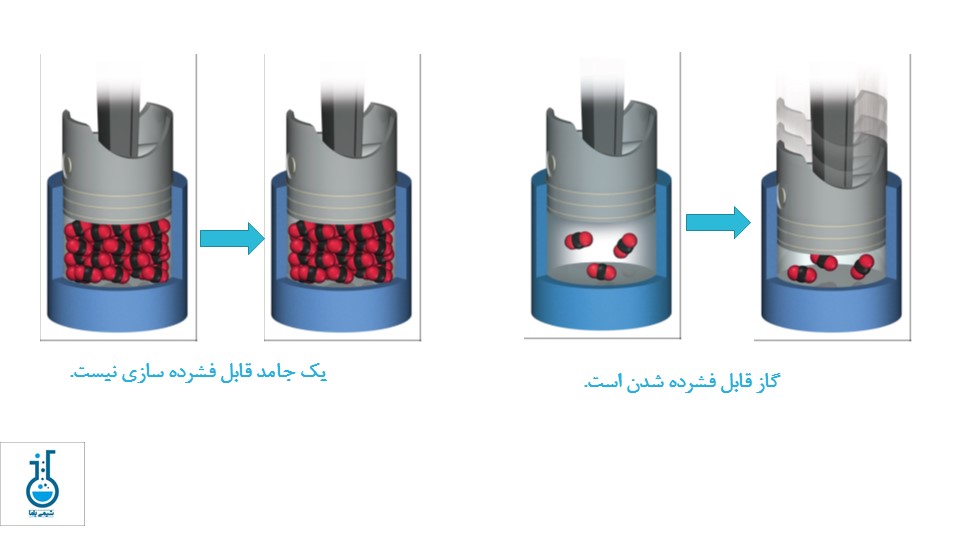
قابلیت فشرده سازی گازها
در یک جامد، اتمها یا مولکولها در مکان خود ثابت هستند و تنها میتوانند ارتعاش کنند. در یک مایع، اگرچه اتمها یا مولکولها نزدیک هم قرار دارند ولی میتوانند از یکدیگر عبور کنند و جریان داشته باشند و شکل ظرف خود را بپذیرند. در یک گاز، اتمها یا مولکولها فاصلههای گستردهای دارند که باعث میشود گازها قابل فشرده شدن و همچنین سیال (قابل جریان یافتن) باشند.
دسته بندی مواد بر اساس ترکیب (اجزای تشکیل دهنده)
ویژگیهای مواد توسط اتمها یا مولکولهایی که آن را تشکیل میدهند تعیین میشود. دستهبندی یک ماده بر اساس ترکیب آن همیشه مشخص نیست و نیازمند این است که ما یا ترکیب واقعی ماده را بدانیم یا بتوانیم آن را در آزمایشگاه آزمایش کنیم. در حال حاضر، ما بر روی مواد نسبتاً متداولی که احتمالاً با آنها برخورد کردهاید، تمرکز داریم. در طبقهبندی ماده، اولین تقسیم بندی ماده بین یک ماده خالص و یک مخلوط است.
ماده خالص
یک ماده خالص تنها از یک جزء تشکیل شده است و ترکیب آن ثابت است (از یک نمونه به نمونه دیگر تغییر نمیکند). اجزای یک ماده خالص میتوانند اتمهای منفرد یا گروههایی از اتمها که به هم متصل شدهاند (مولکولها) باشند. هلیم، آب و نمک سفره (سدیم کلرید) همه مواد خالص هستند.
هر یک از این مواد تنها از یک مولفه تشکیل شدهاند: هلیم از اتمهای هلیم، آب از مولکولهای آب و نمک سفره از واحدهای نمک سدیم کلرید تشکیل شده است. ترکیب یک نمونه خالص از هر یک از این مواد همیشه یکسان است.
انواع ماده خالص
ما مواد خالص را بسته به اینکه آیا میتوانند به مواد سادهتر تجزیه شوند یا نه، به دو نوع – عناصر و ترکیبات – دستهبندی میکنیم.
عنصر
عنصر را نمیتوان به مواد شیمیایی سادهتر تجزیه کرد. هلیم، به عنوان یک ماده خالص، یک مثال خوب برای یک عنصر است.
ترکیب خالص
در یک ترکیب، ماده از دو یا چند عنصر (در مورد آب، هیدروژن و اکسیژن) با نسبت ثابت و معین تشکیل شده است. آب به عنوان یک ماده خالص، یک مثال خوب برای یک ترکیب است.
مخلوط
یک مخلوط،بر خلاف ماده خالص، از دو یا چند جزء تشکیل شده است که نسبت آنها میتواند از یک نمونه به نمونه دیگر متفاوت باشد. به عنوان مثال، چای شیرین که از مولکولهای آب و مولکولهای شکر (با ترکیبی از چند ماده دیگر) تشکیل شده است، یک مخلوط است. ما میتوانیم چای را کمی شیرین کنیم (نسبت کمی از شکر به آب) یا اینکه بسیار شیرین (نسبت زیادی از شکر به آب) یا هر مقدار شیرینی دیگری بین این دو را بسازیم.
انواع مخلوطها
ما همچنین مخلوطها را بسته به میزان یکنواختی مواد درون آنها، به دو نوع – ناهمگن و همگن – دستهبندی میکنیم.
مخلوط ناهمگن
مخلوطهای ناهمگن از فازهای متمایزی تشکیل شدهاند و اتمها یا مولکولهایی که آنها را تشکیل میدهند قابل جداسازی هستند. شن خیس یک مخلوط ناهمگن است، که ترکیب آن در یک نقطه از مخلوط با نقاط دیگر متفاوت است
مخلوط ناهمگن
مخلوطهای همگن ترکیبهای یکنواختی دارند و اتمها یا مولکولهای تشکیل دهنده آنها به صورت یکنواخت مخلوط میشوند. چای شیرین یک مخلوط همگن است، که ترکیب آن در سرتاسر مخلوط یکسان است.

روشهای جداسازی مخلوطها
شیمیدانها اغلب میخواهند اجزای مخلوطها را از هم جدا کنند. اجزا مختلف مخلوطها به دلیل تفاوت در ویژگیهای فیزیکی و شیمیایی قابل جداسازی هستند و جداسازی آنها بسته به اجزای موجود در مخلوط ممکن است به آسانی یا دشواری انجام گیرد. ما میتوانیم با استفاده از تکنیکهای مختلف و بهره گیری از تفاوتهای شیمیایی و فیزیکی، اجزای مختلف یک مخلوط را از هم جدا کنیم. در تصویر زیر انواع مختلفی از تکنیکهای جداسازی آورده شده است.
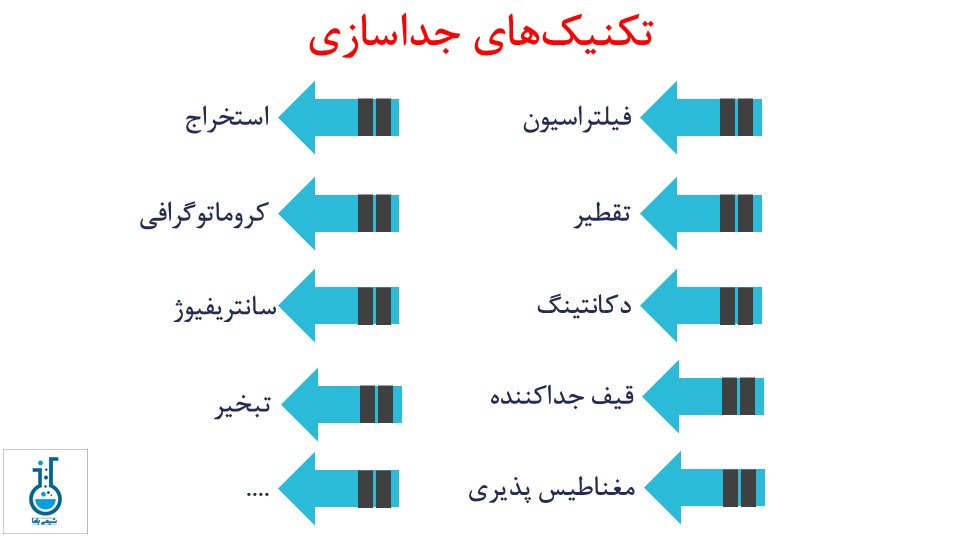
متداولترین تکنیکهایی که به منظور جداسازی مخلوطها در آزمایشگاهها مورد استفاده قرار میگیرند، روشهای دکانتیگ، فیلتراسیون و تقطیر هستند که در ادامه آورده شده است.
دکانتینگ
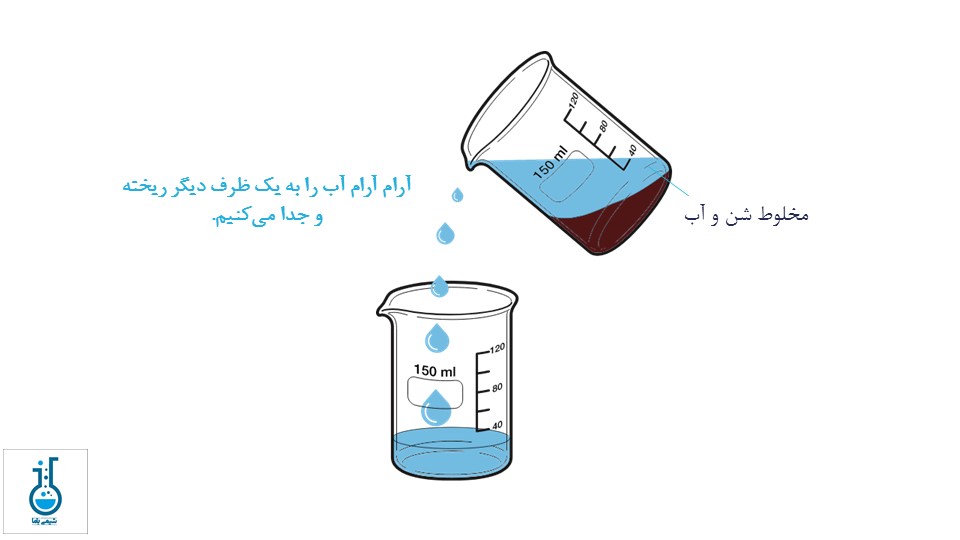
دکانتینگ (decantation) یک روش جداسازی فیزیکی است که برای جداسازی ترکیبات مایع از جامد و مایعات غیرقابل اختلاط (مانند آب و روغن، آب و گازوئیل) مورد استفاده قرار میگیرد. در این فرآیند، مایع بالایی به یک ظرف دیگر منتقل میشود و به این ترتیب ماده جامد یا مایع زیرین از مایع بالایی جدا میشود.
وقتی مخلوط شن و آب را به صورت ساکن قرار دهیم، دو لایه جداگانه تشکیل میشود و شن که سنگینتر است، در پایین و آب در بالا قرار میگیرد . با ریختن لایه آب در یک ظرف دیگر، شن در ظرف اصلی باقی مانده و به این صورت از هم جدا میشوند.
فیلتراسیون
فیلتراسیون (Filtration) یک فرایند جداسازی فیزیکی است که در آن به دلیل قابلیت عبور مایعات از کاغذ صافی، مواد جامد و مایع از یک مخلوط جدا میشوند. زمانیکه مخلوط جامد غیر قابل انحلال و مایع روی کاغذ صافی داخل قیف ریخته میشود، کاغذ صافی جامدات را در خود نگه داشته و ترکیبات مایع عبور کرده و جداسازی میشوند.

تقطیر
فرآیند تقطیر (Distillation) به عنوان یک روش جداسازی فیزیکی، شامل جوشاندن انتخابی یک جزء و متراکم کردن آن به صورت مایع است. از این تکنیک میتوان برای افزایش غلظت یک جزء خاص در مخلوط یا برای جداسازی اجزای (تقریباً) خالص از مخلوط استفاده کرد. اساس فرآیند تقطیر تفاوت در نقطه جوش اجزای مخلوط است. در آزمایشگاه از مجموعهای از تجهیزات برای بستن setup تقطیر استفاده میشود.
انواع تقطیر
برخی از انواع مهم تقطیر شامل موارد زیر هستند:
- تقطیر ساده
- تقطیر جزبه جز
- تقطیر بخار
- تقطیر خلاء
- تقطیر خلاء حساس به هوا
تقطیر ساده
- در فرآیند تقطیر ساده، وقتی که مخلوط همگم مایعات حرارت داده میشوند، مایع دارای نقطه جوش کمتر، سریع تر بخار میشود و در نهایت بخارات سرد و متراکم شده به عنوان مایع خالص جمع آوری میشوند.
- این روش تنها برای مخلوطهایی که نقطه جوش مایعات آنها به طور قابل توجهی متفاوت هستند (حداقل تفاوت 25 درجه سانتیگراد) موثر است.
- خلوص مایع جدا شده توسط قانون رائول (Raoult’s law) مشخص میشود.
- در تصویر زیر شمای کلی فرآیند تقطیر ساده آورده شده است.
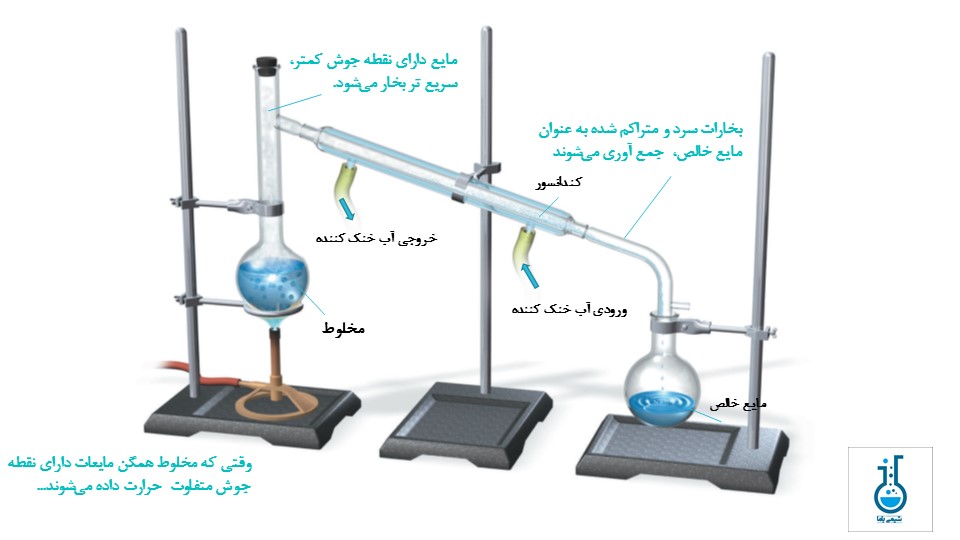
ویدئوی آموزش عملی متداولترین روشهای جداسازی مخلوطها
مراجع
Tro, Nivaldo J. “Principles of chemistry: a molecular approach.” (2020).
Mujtaba, Iqbal M. Batch distillation: Design and operation. Vol. 3. World Scientific Publishing Company, 2004.
Hucknall, David J. Vacuum technology and applications. Elsevier, 2013.


