طیف سنجی تشدید مغناطیسی هسته ای (NMR) یک تکنیک طیف سنجی است که برای دستیابی به اطلاعات ساختاری مولکولها و ترکیبات مجهول استفاده می شود. به منظور دستیابی به اطلاعات و آشنایی با اصول و نحوه تفسیر طیف NMR ضروری است. این تکنیک کاربردهای بسیار گستردهای در زمینههای مختلف شیمی، زیست شناسی، داروسازی، پزشکی و … دارد و پژوهشگران بسیاری از این تکنیک برای شناسایی ترکیبات مجهول استفاده میکنند.

خدمات تفسیر طیف NMR
ما انواع آنالیز NMR شامل 1HNMRو 13CNMR را بررسی و تفسیر می کنیم.
- تفسیر طیف NMR به صورت فارسی و انگلیسی
- تفسیر طیف همراه با ارائه رفرنس و مراجع معتبر
- رسم طیف NMR در نرم افزار اوریجین در صورت درخواست
طیف سنجی NMR بر اساس پدیده فیزیکی تشدید مغناطیسی عمل میکند که ایتدا توسط ایزیدور رابی Isidor I. Rabi در سال 1938 مطرح شده است. برای اولین بار در دهه 1940، دو گروه تحقیقاتی به طور مستقل اولین اندازه گیری موفق NMR را انجام دادند و دو محقق اصلی این گروه ها، فلیکس بلوخ Felix Bloch از دانشگاه استنفورد و ادوارد پرسل Edward M. Purcell از دانشگاه هاروارد موفق شدند به طور مشترک جایزه نوبل فیزیک را در سال 1952 به دلیل تلاشهای خود در این زمینه دریافت کنند.از آن به بعد، همزمان با پیشرفت در زمینههای دیگر مانند ریاضیات، فیزیک و انفورماتیک، طیفسنجی NMR نیز پیشرفت کرد و در دهه 1960با پیاده سازی آهنرباها و رایانه های ابررسانا در تجهیزات آن، پیشرفت زیادی در حساسیت و امکان طراحی انواع جدیدی از آزمایشات NMR حاصل گردید و دانشمندان موفق شدند روشهای جدیدی را برای مطالعه سیستمهای پیچیده، مانند پروتئینهای غشایی، نمونههای پیچیده متابولیکی و حتی بافتهای بیولوژیکی توسعه دهند. امروزه طیفسنجی NMR به یکی از قویترین تکنیکها برای تعیین ساختار ترکیبات شیمیایی و همچنین مطالعه دینامیک مولکولی و برهمکنشها تبدیل شده است.
NMR چیست؟
طیف سنجی NMR یک تکنیک شناسایی فیزیکی شیمیایی بر اساس برهمکنش تابش فرکانس رادیویی خارجی اعمال شده با هسته اتمی است. در طی این برهمکنش یک تغییر انرژی وجود دارد که منجر به ایجاد تغییر در یکی از خواص هستههای اتمی به نام اسپین هستهای nuclear spin میشود.
اسپین هستهای با عدد کوانتومی (I) تعریف می شود که بسته به نوع ایزوتوپ متفاوت است. فقط هستههای اتمی با I≠ 0 در طیفسنجی NMR قابل تشخیص هستند (هستههای فعال NMR، مانند 1H، 19F، 13C و 15N) . این هستههای فعال NMR مانند آهنرباهای کوچک (دوقطبی مغناطیسی) رفتار میکنند که میتوانند با میدانهای مغناطیسی خارجی همسو شوند (فرآیندی به نام مغناطیس پذیری magnetization). نیروی این آهن رباهای کوچک با ثابتی به نام نسبت مغناطیسی (γ) تعریف می شود که مقدار آن به ایزوتوپ بستگی دارد.
اسپینهای هستهای برخی از گونههای فعال NMR زمانی که در میدان مغناطیسی خارجی (B0) قرار میگیرند، میتوانند دو جهتگیری مختلف داشته باشند. یک جهت مربوط به پایین ترین سطح انرژی هسته (موازی با میدان مغناطیسی خارجی) و دیگری مربوط به بالاترین سطح انرژی هسته (در جهت مخالف میدان مغناطیسی خارجی) است (شکل 1، سمت چپ). تفاوت بین سطوح انرژی (ΔE) به میدان مغناطیسی و نسبت مغناطیسی پذیری بستگی دارد و در حساسیت تکنیک تأثیر گذار است. (شکل 1، سمت راست).
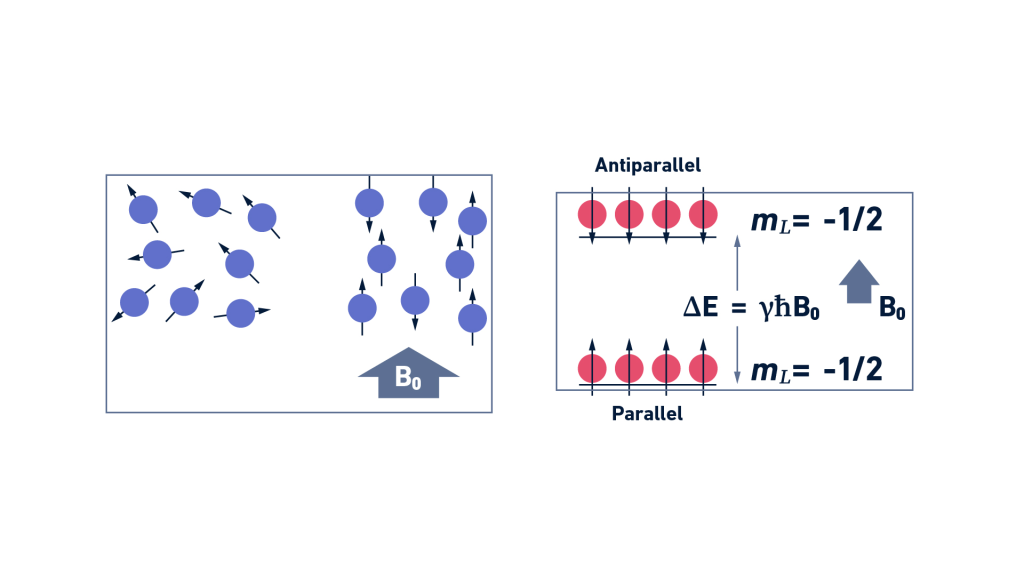
رزونانس مغناطیسی زمانی حاصل می شود که هستهها تحت امواج رادیو فرکانس قرار گیرند. این امر باعث انتقال بین سطوح انرژی و تغییر جهتگیری اسپینهای هسته ای می شود.
وقتی هستههای اتمی تحت تأثیر میدان مغناطیسی قرار میگیرند، دوقطبیهای مغناطیسی هستهای بهطور ایستا با میدان مغناطیسی B0 همتراز نیستند و مانند یک نوک چرخان حول محوری موازی با جهت میدان حرکت میکنند (شکل 2، سمت چپ). فرکانس این حرکت تقدیمی precession movement که فرکانس لارمور Larmor frequency (νL) نامیده می شود، با نسبت مغناطیسی و میدان مغناطیسی تعریف می شود:
در نتیجه این حرکت تقدیمی، بردار مغناطیسی (μ) متناسب با دوقطبی های مغناطیسی هسته دارای یک مؤلفه موازی با میدان مغناطیسی (μz) و یک مؤلفه عمود بر میدان مغناطیسی (μxy) است که در غیاب میدان مغناطیسی دارای مقدار صفر است. در آنالیز NMR، اندازه گیری سیگنال در جهت z امکان پذیر نیست، زیرا میدان مغناطیسی در آن جهت بسیار شدید است. بنابراین لازم است مغناطیس پذیری مولفه z به صفحه xy منتقل شود. برای این منظور، یک پالس مغناطیسی حاوی فرکانسهای نزدیک به فرکانس لارمور عمود بر B0 اعمال میشود که منجر به رزونانس اسپینهای هستهای و تولید μxy غیرصفر میشود.
پس از این پالس، یک فرآیند آسایش صورت گرفته و جزء μxy به مقدار صفر میرسد (شکل 2، سمت راست). در نتیجه این آسایش، انرژی به عنوان فرکانس رادیویی ساطع می شود و سیگنال ویژهای به نام واپاشی القایی آزاد (FID) free induction decay تولید می کند که توسط آشکارساز ثبت می شود. این FID متعاقباً به نموداری از شدت ها در مقابل فرکانس هایی که به عنوان طیف NMR شناخته می شود، تبدیل می شود.
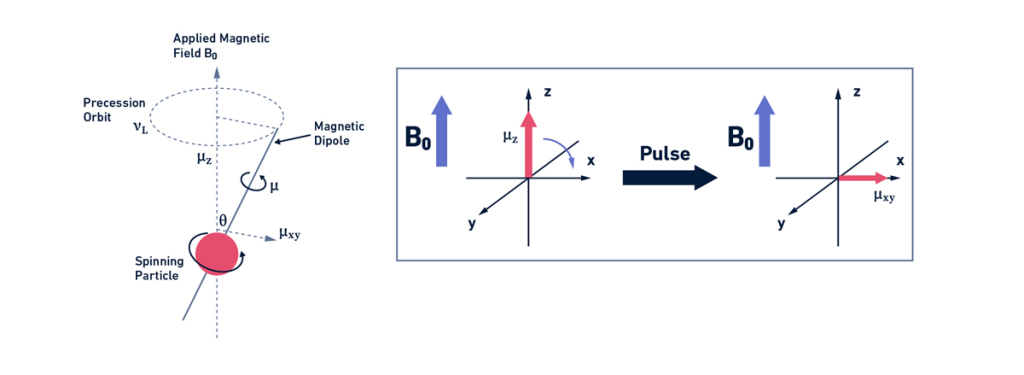
شکل 2: رفتار اسپین هسته ای تحت تأثیر میدان مغناطیسی خارجی (سمت چپ). شمای یک آنالیز NMR پایه که در آن مغناطیس پذیری با اعمال یک پالس مغناطیسی به صفحه xy منتقل می شود (سمت راست).
NMR چگونه کار می کند؟
طیف سنج های NMR از سه جزء اصلی تشکیل شده اند:
- آهنربای ابررسانا (superconducting magnet)
- پروب (probe)
- سیستم الکترونیکی پیچیده (console) که توسط اپراتور کنترل می شود (شکل 3).
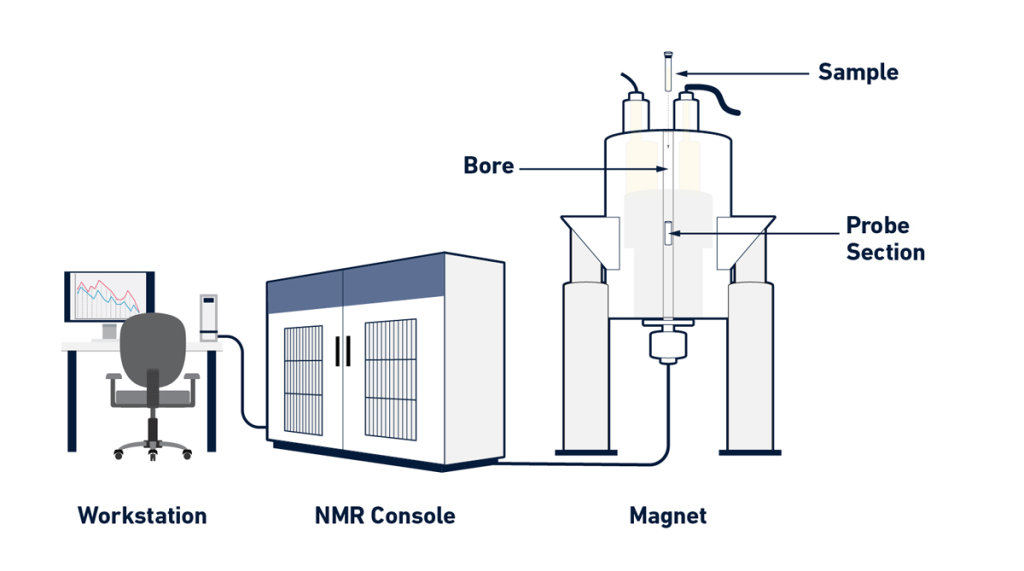
آهنربای ابررسانا (superconducting magnet)
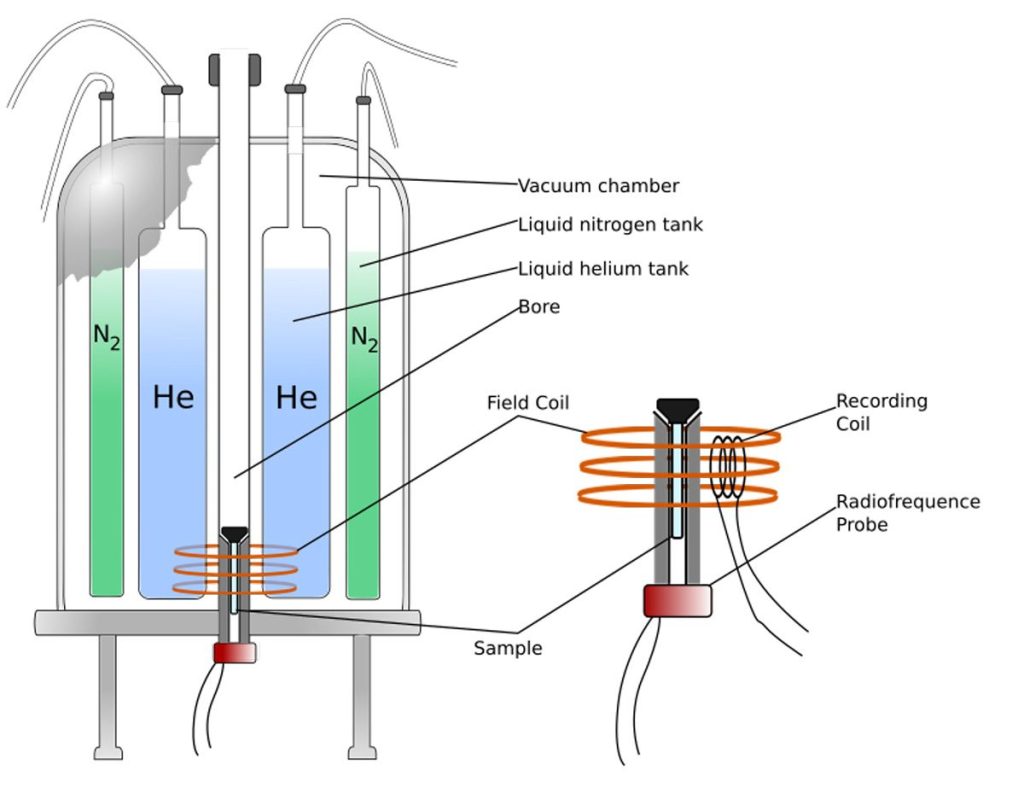
آهنربا مسئول تولید یک میدان مغناطیسی قوی است که اسپین های هسته ای اتم های موجود در نمونه را هم تراز می کند. امروزه آهنرباهای مورد استفاده در طیف سنجی NMR بر اساس مواد ابررسانا هستند و برای کار کردن به دمای بسیار پایینی (حدود 4K ) نیاز دارند. به همین دلیل، طیفسنجهای NMR شامل یک سیستم خنککننده متشکل از یک پوشش داخلی پر از هلیوم مایع است که توسط یک پوشش اضافی پر از نیتروژن مایع، و لایههای زیادی از مواد عایق حرارتی در یخچال نگهداری میشود (شکل 4).
پروب (probe)
آهنربای ابررسانا محفظه ای استوانه ای به نام “پروب” را احاطه کرده است که مهمترین جزء NMR است. نمونه وارد پروب می شود و تحت تأثیر میدان مغناطیسی قرار می گیرد. پروب حاوی یک سری سیم پیچهای مغناطیسی است که در اطراف نمونه قرار دارند (شکل 4). این سیم پیچها اهداف متعددی دارند و به منظور تابش پالسهای فرکانس رادیویی و شناسایی و جمع آوری سیگنال NMR ساطع شده توسط نمونه و همچنین به منظور کنترل همگن بودن میدان مغناطیسی و اعمال گرادیان پالس که در برخی از آزمایشهای NMR استفاده میشوند، مورد استفاده قرار میگیرند.
سیستم الکترونیکی پیچیده (console)
در نهایت، سیستم الکترونیکی طیفسنج تمام شرایط آزمایشی را کنترل میکند و تنظیم و اصلاح هر پارامتر آزمایش NMR را از طریق اپراتور امکانپذیر میسازد. این سیستم همچنین مسئول جمع آوری داده ها و تبدیل ریاضی آنها به طیف NMR است. این طیف شامل یک سری پیک با شدت های مختلف به عنوان تابعی از بزرگی است که به عنوان جابجایی شیمیایی chemical shift شناخته می شوند و از فرکانس لارمور هسته های مختلف اتمی موجود در نمونه به دست می آید.
نحوه تفسیر طیف NMR
سیگنال شناسایی شده توسط یک طیف سنج NMR (FID) قبل از تجزیه و تحلیل، بایستی تبدیل ریاضی شود زیرا فرکانس لارمور به شدت میدان مغناطیسی بستگی دارد و در دستگاههای مختلف، متفاوت است. به همین دلیل، یک تبدیل ریاضی برای دستیابی به یک مقدار نسبی به نام جابجایی شیمیایی (δ) انجام میشود . برخلاف فرکانس لارمور، جابجایی شیمیایی مستقل از میدان مغناطیسی است و می توان مقادیر حاصل از دستگهای مختلف را باهم مقایسه کرد.
از آنجایی که νL فرکانس لارمور مشاهده شده یک هسته و νL0 فرکانس لارمور هسته مرجع بر حسب هرتز است. طبق قرارداد، جابجایی شیمیایی همیشه بر حسب قسمت در میلیون (ppm) بیان می شود. مقدار صفر جابجایی شیمیایی با استفاده از یک ترکیب مرجع (مانند تترمتیل سیلان (TMS) یا تری متیل سیلیل پروپان سولفونات سدیم (DSS) برای 1H تنظیم می شود.
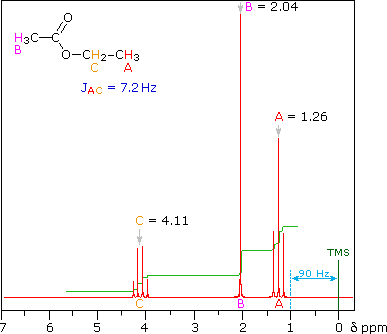
شکل 5 نمونه ای از طیف پروتون 1H NMR را ارائه می دهد، به این معنی که فقط پروتون های مولکول شناسایی می شوند.
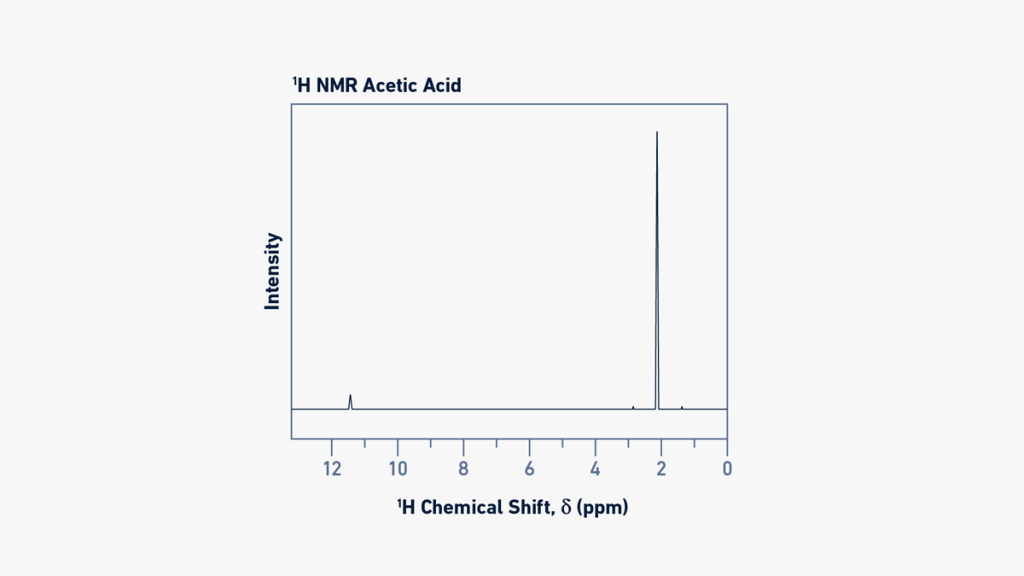
یک طیف NMR اطلاعات زیادی در مورد مولکول های موجود در نمونه ارائه می دهد. ابتدا، گروه های شیمیایی درون یک مولکول را می توان از روی مقادیر جابجایی شیمیایی شناسایی کرد. در مثال ارائه شده در شکل 5، اسید استیک (H3C-COOH) دارای چهار پروتون است، بنابراین شما می توانید انتظار دیدن چهار سیگنال در طیف را داشته باشید. با این حال، سه پروتون گروه متیل (CH3) از نظر مغناطیسی معادل هستند و بنابراین جابجایی شیمیایی یکسانی دارند. این بدان معنی است که یک سیگنال مربوط به گروه CH3 و دیگری مربوط به پروتون گروه کربوکسیلیک اسید (COOH) است.
ثانیاً، در طیفهای 1H-NMR، مساحت سیگنال متناسب با تعداد هستههای اتمی است که آن سیگنال را تولید میکنند (این در مورد طیفهای 13C-NMR صدق نمیکند). در این مثال، اگر قرار باشد مساحت هر دو سیگنال محاسبه شود، شدیدترین سیگنال سه برابر بزرگتر از دیگری خواهد بود. این مطابق با این واقعیت است که یک سیگنال نشان دهنده سه پروتون از گروه CH3 (سیگنال در δ = 2.0 ppm) و دیگری پروتون از گروه COOH (سیگنال در δ = 11.5 ppm) است.
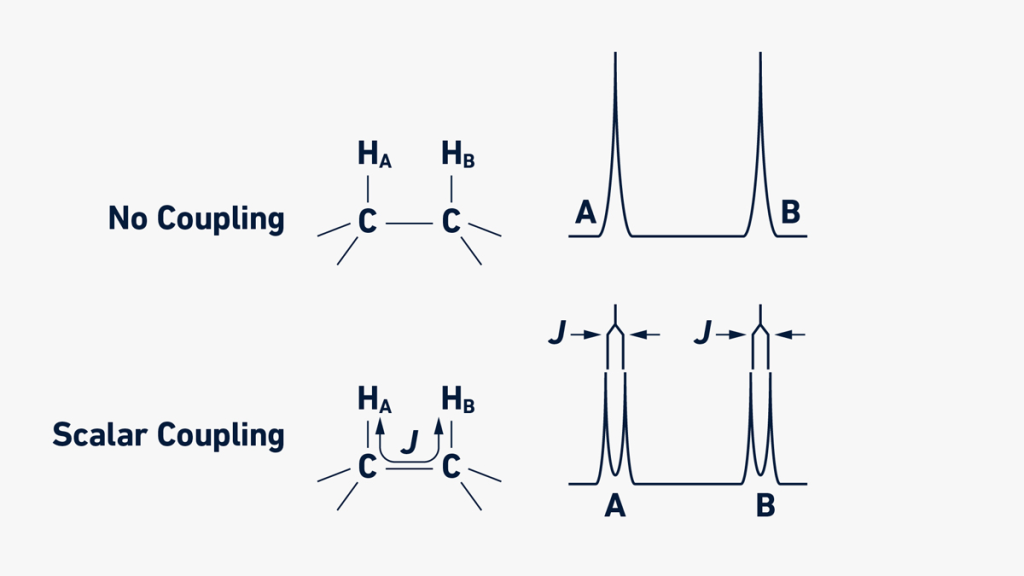
اسپین های دو هسته که از طریق چند پیوند شیمیایی به هم متصل شده اند می توانند برهم کنش داشته باشند و باعث ایجاد پدیده ای به نام کوپلاژ اسکالر scalar coupling شوند که سیگنال ها را شکافته می کند. به طور معمول، این کوپلاژ تنها زمانی قابل مشاهده است که تعداد پیوندهای شیمیایی جداکننده دو هسته از چهار تجاوز نکند. تقسیم سیگنال ها از الگویی پیروی میکند که به تعداد هسته های جفت شده و ثابت کوپلاژ (J) که توسط نوع هسته ها و فاصله (در پیوندهای شیمیایی) بین آنها تعریف می شود، بستگی دارد.
شکل سیگنال شکافته شده، چندگانگی (multiplicity) نامیده می شود و اطلاعات مهمی را در مورد مولکول ارائه می دهد. این چندگانگی را می توان با استفاده از قانون N+1 محاسبه کرد. این قانون بیان می کند که اگر یک پروتون با N پروتون های متصل به هستههای کربنی کوپلاژ داشته باشد، سیگنال آن به قله های N+1 با شدت نسبی که توسط مثلث پاسکال Pascal’s triangle تعریف شده است شکافته می شود (شکل 6). شکافته شدن پیک به دلیل کوپلاژ اسکالر باعث کاهش شدت پیک می شود.
برای تفسیر یک طیف NMR بایستی از تمام اطلاعات آن برای اختصاص دادن سیگنال مشاهده شده به هسته اتمی مولکول(های) نمونه استفاده شود. این فرآیند تخصیص طیفی spectral assignment نامیده میشود. تخصیص طیفی در مولکولهای پیچیده تر دشوارتر است و به همین دلیل، معمولا از انواع مختلف آزمایشات NMR استفاده میکنند تا بتوانند به اطلاعات متفاوت و مکمل برای توصیف یک نمونه دست یابند.
جابجایی بالا (Upfield ) و جابجایی پایین (downfield) در NMR
همانطور که در شکل 5 مشاهده می شود، هسته های مشابه می توانند سیگنال هایی با مقادیر شیفت شیمیایی متفاوت تولید کنند. علت متفاوت بودن این تغییرات شیمیایی این است که میدان مغناطیسی احساس شده توسط یک هسته خاص به شدت به محیط شیمیایی محلی آن بستگی دارد. گردش الکترون ها در اطراف یک هسته، میدان های مغناطیسی کوچکی را ایجاد می کند که در جهت مخالف میدان خارجی اعمال شده است. این اثر شیلد shielding effect (σ) مستقیماً به چگالی الکترونیکی اطراف هسته وابسته است و منجر به کاهش میدان مغناطیسی موثر بر روی هسته و تحت تاثیر قرار گرفتن فرکانس لارمور میشود.
هنگامی که یک چگالی الکترونیکی بالا در اطراف هسته وجود داشته باشد اثر شیلد، زیاد است و فرکانس لامور کاهش می یابد و به جابجایی شیمیایی کاهش می یابد (به سمت میدان بالا upfield (سمت راست) حرکت می کند). برعکس، هنگامی که چگالی الکترونیکی در مجاورت هسته کم است، اثر شیلد کم است و فرکانس لارمور مقادیر بالاتری می گیرد و به همین ترتیب شیفت شیمیایی مشاهده میشود (به سمت پایین downfield (سمت چپ) حرکت می کند)..
بنابراین، در طیفسنجی NMR، اصطلاحات upfield و downfield به ترتیب به جابجایی شیمیایی به سمت مقادیر پایینتر و بالاتر اشاره دارند (شکل 7).
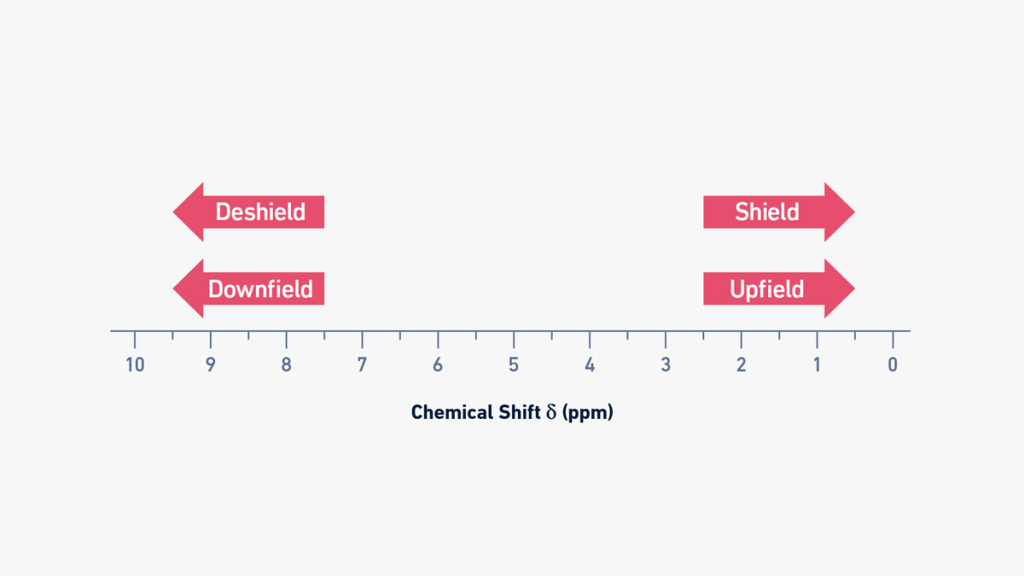
شکل 7: مقیاس جابجایی شیمیایی 1H NMR که مناطق رو به پایین و بالا را نشان می دهد.
هستههای هیدروژن گروههای متیل یا مولکولهای آلیفاتیک به شدت شیلد میشوند و مقادیر جابجایی شیمیایی معمولی آنها در upfield (راست) مشاهده میشود. از سوی دیگر، هستههای هیدروژن متصل به اتمهای الکترونگاتیو (مانند اکسیژن یا نیتروژن) یا نزدیک به گروههای الکترونگاتیو (مانند اسیدهای کربوکسیلیک یا آلدئیدها) لایهپوشی میشوند و جابجایی شیمیایی را در downfield (چپ) نشان میدهند. این در بخش بعدی نمودارهای NMR نشان داده و بیشتر مورد بحث قرار گرفته است.
ما روی داده های شما کار می کنیم تا اطلاعات مفید را استخراج و تفسیر کنیم!
چرا ما را انتخاب کنید؟
پشتیبانی 24 ساعته در 7 روز هفته
تجزیه و تحلیل دقیق توسط متخصصین
تضمین کیفیت و رضایت
بازبینی رایگان پس از تکمیل سفارشات
قیمت مناسب
پروتون NMR و کربن NMR
عناصر اصلی تشکیل دهنده مولکول های آلی و بیولوژیکی هیدروژن و کربن هستند. همانطور که در بالا توضیح داده شد، طیفسنجی NMR را فقط میتوان بر روی هستههای فعال NMR (یعنی هستههایی با I≠ 0) اعمال کرد. فراوان ترین ایزوتوپ هیدروژن در NMR فعال است ( ½=1H, 99.98%, I) ولی فراوان ترین ایزوتوپ کربن در NMR فعال نیست (12C، 98.89٪، I = 0) و طیفسنجهای NMR فقط میتوانند ایزوتوپ 13C را شناسایی کنند که فراوانی1.11% دارد. علاوه بر این، نسبت مغناطیسی 13C نیز چهار برابر کمتر از 1H است. این عوامل باعث می شوند حساسیت 13C-NMR به طور قابل توجهی کمتر از 1H-NMR باشد و زمان های آزمایش 13C (ساعت) در مقایسه با 1H (ثانیه یا دقیقه) طولانی تر شود.
جابجایی شیمیایی 1H معمولاً در محدوده 0 تا 14ppmاتفاق میافتد، در حالی که جابجاییهای شیمیایی 13C در محدوده بسیار بزرگتری، معمولاً 10 تا 22ppm رخ میدهد. این وابستگی مقادیر جابجایی شیمیایی به نوع هستهها از این واقعیت ناشی میشود که هستههای مختلف دارای فرکانسهای لامور متفاوتی هستند (همانطور که قبلاً ذکر شد به نسبت مغناطیسی بستگی دارد). این جابجایی بالا در 13C-NMR منجر به وضوح بهتر در مقایسه با 1H-NMR میشود و معمولاً سیگنالها پراکندهتر هستند.
همچنین، کوپلاژ اسکالر در 13C به ندرت مشاهده می شود زیرا، به دلیل فراوانی طبیعی کم، بعید است که دو اتم 13C به اندازه کافی نزدیک باشند تا بتوانند بین اسپین های هسته ای خود برهمکنش داشته باشند. با این حال، جفت شدن اتم های 13C با هسته های دیگر امکان پذیر است و می تواند حساسیت این تکنیک را بیشتر کاهش دهد. دلیل این امر هم بزرگ بودن ثابتهای کوپلاژ 13C است و زمانی که ثابتهای کوپلاژ بزرگ هستند کاهش شدت سیگنال در هنگام تقسیم بیشتر مشخص میشود. به همین دلیل، آزمایشهای 13C-NMRمعمولاً با استفاده از توالیهای پالس خاصی انجام میشوند تا کوپلاژ اسکالر بین 13C و 1H حذف شوند. البته با استفاده از روشهای مختلف میتوان حساسیت 13C-NMR را بهبود بخشید.
علیرغم محدودیت های 13C-NMR، این تکنیک اطلاعات ارزشمندی را ارائه می دهد که حصول آنها با استفاده تنها از 1H-NMR امکان پذیر نیست. از جمله این موارد شناسایی انواع اتمهای کربن است، اغلب مواقع، 13C-NMR و 1H-NMR به طور مشترک برای تعیین ساختار مولکولی استفاده می شوند.
طیف NMR
طبق قرارداد، مقیاس تغییر شیمیایی در یک طیف NMR از راست به چپ نشان داده می شود. همانطور که در بالا توضیح داده شد، مقدار صفر با استفاده از یک ترکیب استاندارد ایجاد می شود که اتم های کربن و هیدروژن آن به شدت شیلد می شوند و سیگنال های آنها در دورترین ناحیه upfield ظاهر می شوند (همانطور که در شکل 7 مشاهده می شود). به منظور تسهیل شناسایی سیگنال NMR، تخصیص طیف های NMR معمولاً با کمک نمودارهای NMR انجام می شود.
هیدروژنها یا کربنهایی که به شدت شیلد میشوند، مانند گروههای متیل، مقادیر جابجایی شیمیایی پایینی دارند ولی هیدروژن های متصل به گروه های بسیار الکترونگاتیو (به عنوان مثال، اسیدهای کربوکسیلیک، کتون ها یا آلدئیدها) دارای مقادیر جابجایی شیمیایی بالایی هستند (شکل های 8 و 9).
این نمودارها تغییرات شیمیایی معمولی را نشان میدهند، اما گاهی اوقات این مقادیر میتوانند به مناطق دیگر مقیاس جابهجا شوند. برای مثال، در ماکرومولکولهای بزرگ، یک گروه شیمیایی دورتر از هسته مدنظر میتواند به دلیل آرایش فضایی ساختار سهبعدی جابجا شده و باعث تغییر محیط شیمیایی هسته اندازه گیری شده و تغییر جابجایی شیمیایی آن شود.
به منظور تسهیل تخصیص طیف NMR، کتابخانهها یا پایگاههای اطلاعاتی عمومی NMR (مانند Biological Magnetic Resonance Data Bank یا Spectral Database for Organic Compounds) وجود دارد که حاوی طیفهای NMR و مقادیر تغییر شیمیایی برای هزاران مولکول بیوشیمیایی و ترکیبات شیمیایی است.
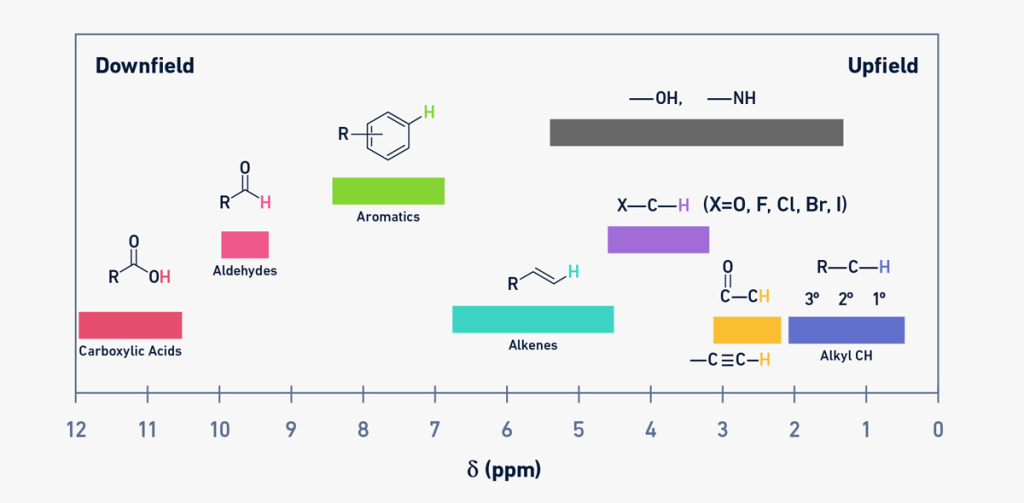
شکل 8: نمودار 1H-NMR که مقادیر جابجایی شیمیایی را برای انواع مختلف اتم های هیدروژن نشان می دهد.
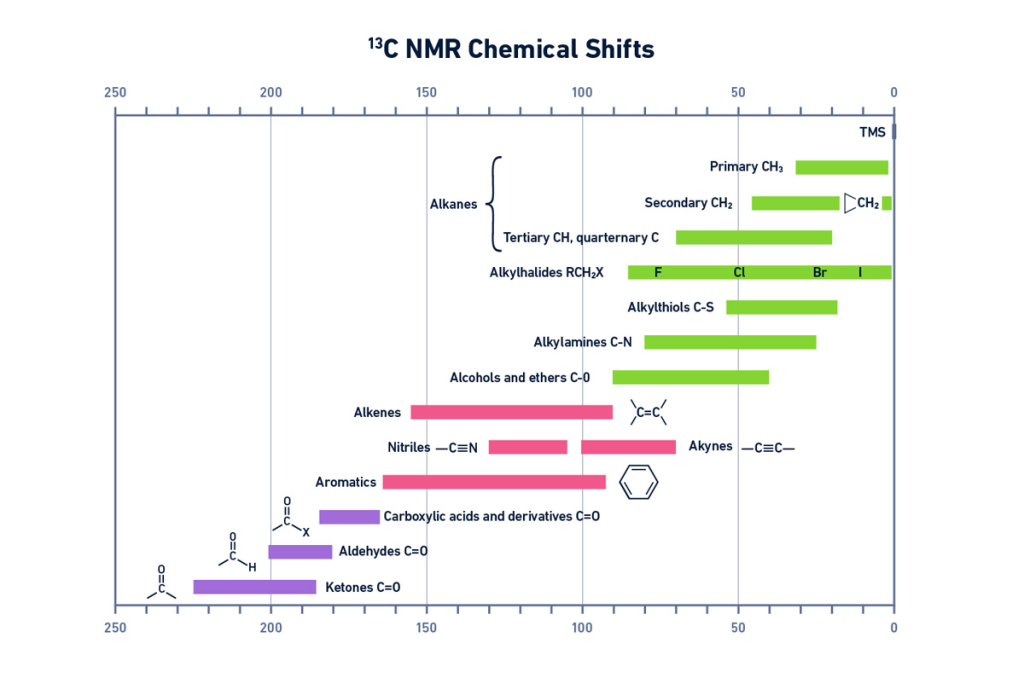
شکل 9: نمودار 13C-NMR که مقادیر جابجایی شیمیایی را برای انواع مختلف اتمهای کربن نشان میدهد.
انواع NMR
پالس های مغناطیسی به کار رفته در NMR به طور گسترده در طول زمان توسعه یافته اند به طوری که در حال حاضر تعداد بی شماری انواع آزمایش های NMR وجود دارند که برای به دست آوردن مقدار زیادی اطلاعات در مورد نمونه های مختلف استفاده میشوند. دو مورد از رایج ترین انواع آن، NMR دو بعدی (2D ) و NMR حالت جامد هستند.
۱. NMR دو بعدی (2D )
درشت مولکولها، مانند پروتئینها، تعداد زیادی هستههای فعال NMR دارند و در نتیجه، طیفهای NMR آنها پیچیده است که بسیاری از پیکها باهم همپوشانی دارند. علاوه بر این، آسایش در مولکول های بزرگ سریعتر است، که منجر به کاهش وضوح طیف میشود. برای رفع این محدودیتها، NMR دوبعدی طیفهایی را تولید میکند که دارای دو محور جابجایی شیمیایی (به جای یک محور جابجایی شیمیایی، مانند طیفهای NMR تک بعدی) هستند و سیگنالهای مربوط به کوپلازهای هستهای مختلف را به هم مرتبط میکنند. سه مورد از انواع NMR دو بعدی عبارتند از COSY، TOCSY و NOESY.
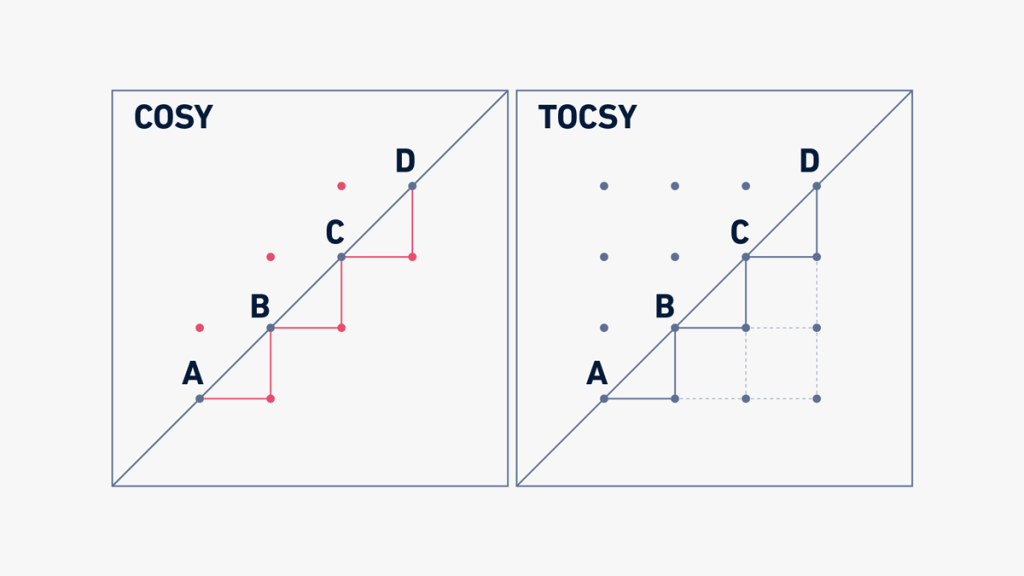
طیف COZY (Correlated SpectroscopY) سیگتالهایی را نشان میدهد که شامل ارتباط کوپلاژ هستههایی با حداکثر سه پیوند شیمیایی هستند. این همبستگی از تعامل بین اسپین های هسته ای از طریق کوپلاژ اسکالر ناشی می شود (شکل 10).
طیف های TOCSY (Total Correlated SpectroscopY) سیگنال هایی را نشان می دهند که مربوط به جفت شدن هسته های یک سیستم اسپینی هستند (یک سیستم اسپین مجموعه ای از هستههایی است که اسپین های آنها با یکدیگر برهمکنش داشته و کوپل شده اند) (شکل 10).
طیف NOESY (Nuclear Overhauser Effect SpectroscopY) در تعیین ساختاری درشت مولکولها بسیار مهم هستند زیرا اطلاعاتی درباره سازمان فضایی آنها ارائه میدهند. طیفهای NOESY حاوی سیگنالهایی هستند که جفتهای هستههای مجاور را به هم مرتبط میکنند. برخلاف COSY، همبستگی NOESY از اثر Overhauser هسته ای ناشی می شود، که در آن برهمکنش بدون توجه به تعداد پیوندهای شیمیایی که آنها را از هم جدا می کند، زمانی رخ می دهد که دو هسته از نظر مکانی به هم نزدیک باشند، .
۲. NMR حالت جامد
علیرغم این واقعیت که بیشتر آنالیزهای NMR بر روی نمونه های محلول انجام می شود، استفاده از NMR حالت جامد به طور قابل توجهی در دهه گذشته توسعه یافته است. NMR حالت جامد یکی از قویترین تکنیکها برای مطالعه ساختارهای مولکولی و دینامیک در نمونههای جامد است. این نوع NMR ویژگی های خاصی داشته و نیاز به روشهای آزمایشی متفاوتی دارد.
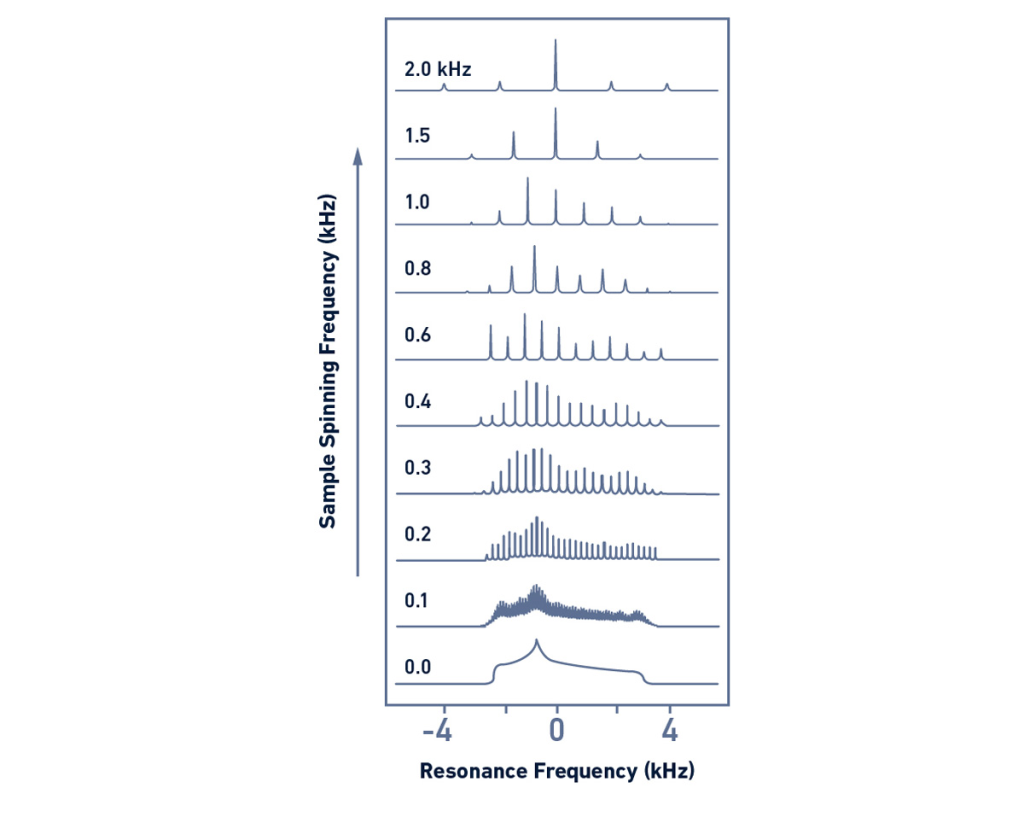
NMR محلول و NMR حالت جامد تفاوتهای قابلتوجهی را نشان میدهند، عمدتاً به این دلیل که مولکولهای موجود در محلول قادر به حرکت آزادانه هستند و برهمکنشهای اسپین هستهای بهطور متوسط محاسبه میشوند ولی در نمونههای جامد، حرکت مولکولی کمی وجود دارد یا اصلاً وجود ندارد و در نتیجه، برهمکنشهای اسپین هستهای به جهت فضایی بستگی دارد (برهمکنشهای ناهمسانگرد anisotropic interactions). این ناهمسانگردی باعث پهن شدن سیگنال های طیفی NMR می شود (شکل 11، طیف پایین). به همین علت، دانشمندان برای استفاده از NMR حالت جامد، تکنیکهای خاصی را توسعه دادهاند که باعث افزایش حساسیت و وضوح میشوند.
شناخته شده ترین روش NMR حالت جامد، چرخش با زاویه جادویی (MAS) magic angle spinning است. این تکنیک شامل قرار دادن نمونه در داخل یک روتور است که با سرعت بالا می چرخد و یک زاویه خاص (زاویه جادویی ≈54.74º) با توجه به جهت میدان مغناطیسی خارجی تشکیل می دهد. در اثر این چرخش، تمام برهمکنشهای اسپین ناهمسانگرد (شامل برهمکنشهای دوقطبی، ناهمسانگردی شیفت شیمیایی و چهار قطبی) از بین میروند (شکل 11).
نقاط قوت و ضعف NMR
طیف سنجی NMR یک تکنیک قدرتمند است که مزایای زیادی نسبت به سایر تکنیک ها دارد، اما محدودیت هایی نیز دارد که به طور خلاصه در جدول ۲ خلاصه شده است.
جدول 2: خلاصهای از نقاط قوت و ضعف اصلی طیف سنجی NMR.
| نقاط قوت | نقاط ضعف |
|---|---|
| قابل استفاده برای انواع مختلف نمونه: محلولها، جامدات، بافتها، گاز | فقط هسته هایی با I≠ 0 قابل اندازه گیری هستند |
| طیف وسیعی از اطلاعات را ارائه می دهد: ساختار مولکولی، دینامیک، برهمکنش ها، پارامترهای فیزیکی، اندازهگیری کمی | حساسیت کم |
| مولکولها در حالت اصلی خود اندازه گیری میشوند. | برخی از آزمایشات زمان بر هستند |
| شناسایی آسان ترکیب مجهول با استفاده از کتابخانه های NMR | ناهمگنی میدان مغناطیسی باید اصلاح شود |
| آماده سازی نمونه آسان و ارزان | بهینه سازی دستگاه قبل از اندازه گیری مورد نیاز است |
| تکنیک غیر مخرب | تخصیص طیفی و تفسیر دادهها می تواند در برخی از انواع نمونهها پیچیده باشد |
| تکرارپذیری بالا | احتمال تداخل طیفی ناخالصی ها و حلال ها |
ناخالصیهای NMR
یکی از رایج ترین مشکلاتی که در طیف سنجی NMR با آن مواجه می شود، احتمال تداخل مواد، مانند ردپای ناخالصی ها یا حلال ها است که باعث پیدایش پیک های نامطلوب در طیف می شود.
آنالیتهای موجود در نمونههای NMR معمولاً با فرآیند سنتز ویا خالصسازی به دست میآیند که در آن بسیاری از مواد دخیل هستند. به همین دلیل، احتمال وجود برخی مواد ناخالصی در آنها وجود دارد. گاهی اوقات، آنالیت دچار تغییر یا تخریب می شود که می تواند منجر به ظهور گونه های شیمیایی نامطلوب در نمونه گردد. اگر این ناخالصی ها دارای هسته های فعال NMR باشند، می توانند باعث ایجاد مشکل در تفسیر طیف NMR شوند. به طور کلی، ناخالصی های NMR در غلظت کمی یافت می شوند و شناسایی آنها نسبتاً آسان است و پیک های آن ها در مقایسه با آنالیت، شدت بسیار پایینی دارند. برای سهولت در شناسایی ناخالصی ها، آزمایشگاه ها اغلب از جداولی استفاده می کنند که جابجایی شیمیایی رایج ترین ناخالصی ها را نشان میدهند.
پیک حلال NMR
حلالهای مورد استفاده در طیفسنجی NMR معمولاً حاوی هستههای فعال NMR، به ویژه 1H هستند و میتوانند باعث تداخل در طیفهای NMR شوند. بر خلاف ناخالصی های ناچیز، حلال در نمونه با غلظت بسیار بالایی وجود دارد و پیک های ناشی از آن معمولاً بسیار بلند هستند. بنابراین، بسیار مهم است که دقیقاً جابجایی شیمیایی پیک های حلال را بدانیم تا بتوانیم همپوشانی آن با سیگنال آنالیت مورد نظر را بررسی کنیم. یکی از راههای کاهش اثر پیک حلالهای حاوی هیدروژن، استفاده از حلالهای دوتره شده است که شدت پیک های حلال را به میزان قابل توجهی کاهش می دهد. همچنین برخی از پالسهای NMRنیز هستند که میتوانند همپوشانیهای پیک حلال را در طیفهای NMR کاهش دهند.
کاربردهای NMR
طیف سنجی NMR به طور گسترده در زمینه های مختلفی از جمله شیمی و زیست شناسی کاربرد دارد.
کاربردهای NMR در شیمی
کاربرد اصلی طیفسنجی NMR در شیمی شناسایی و توصیف ساختاری مولکولهای آلی، آلی فلزی و بیوشیمیایی است. شناسایی ترکیبات با استفاده از NMR با دادههای به دست آمده از تکنیک های دیگر، مانند طیف سنجی جرمی، طیف سنجی IR، طیفسنجی فرابنفش-مرئی و آنالیز عنصری تکمیل میشود. همچنین، تناسب بین مساحت سیگنالها و تعداد هستههایی که آن را تولید میکنند، این امکان را فراهم میکند تا بتوان از طیفسنجی NMR به عنوان یک ابزار تحلیل کمی استفاده کرد. برخی از نمونههای کاربرد NMR در زمینههای مرتبط با شیمی عبارتند از:
شیمی : تعیین ساختاری ترکیبات جدید، کنترل کیفیت محصولات و تعیین خلوص مواد.
داروسازی: مطالعه ساختار، دینامیک و فعل و انفعالات مولکولی، کنترل کیفیت و تعیین خلوص داروها.
پتروشیمی: تجزیه و تحلیل مواد برای بررسی مناسب بودن مخزن نفت مورد بهره برداری، تجزیه و تحلیل ترکیب NMR حالت جامد مشتقات نفتی، کنترل کیفیت محصولات.
مواد: مشخصات مواد جدید توسط NMR حالت جامد.
کاربردهای NMR در علوم زیستی
در زیست شناسی، طیفسنجی NMR به طور گستردهای برای تفکیک ساختاری ماکرومولکولهای بیولوژیکی از جمله پپتیدها، پروتئینها، لیپیدها، کربوهیدراتها و اسیدهای نوکلئیک استفاده میشود. این سیستم ها بسیار پیچیده هستند لازم است که از تدابیر خاصی برای آنها در نظر گرفته شود که شامل موارد زیر هستند:
- نشانه گذاری ایزوتوپی برای غنی سازی نمونه
- استفاده از پالس های NMR ویژه برای کاهش همپوشانی سیگنال و افزایش وضوح
- استفاده از آزمایشهای NMR با ابعاد بالا (2 بعدی، سه بعدی یا حتی بالاتر)
بعد از حصول طیف NMR، داده های به دست آمده برای به دست آوردن اطلاعات در مورد جابجایی های شیمیایی، زوایای پیچش و فاصله بین اتم ها پردازش می شوند. سپس از این اطلاعات برای دستیابی به ساختار مولکولی با استفاده از نرم افزارهای کامپیوتری توسعه یافته استفاده میشود.
در کنار تبیین ساختاری، طیفسنجی NMR همچنین میتواند برای استخراج اطلاعات در مورد دینامیک مولکولی مانند زمانهای آسایش، ویژگیهای ساختاری و برهمکنشهای بین مولکولها استفاده شود. همچنین NMR حالت جامد برای مطالعه پروتئینهای یا سایر سیستمهای بیولوژیکی که مانند فاز متراکم عمل میکنندمفید است.
چند نمونه از کاربردهای NMR در زمینه های مرتبط با علوم زیستی عبارتند از:
بیولوژی مولکولی و بیوفیزیک: مطالعه ساختار، دینامیک و برهمکنشهای مولکولی پپتیدها، پروتئینها، اسیدهای هسته، کربوهیدراتها و سایر مولکولهای زیستی
پزشکی: تجزیه و تحلیل مایعات بیولوژیکی جهت بررسی بیماریها، استفاده از تصویربرداری NMR برای تشخیص پزشکی
علوم غذایی: بررسی کیفیت یا اصالت نمونههای غذا، نوشیدنی و ….
نتیجه گیری
در این مقاله سعی کردیم تا شما را با اصول طیف سنجی NMR، نحوه تفسیر طیف NMR و کاربردهای آن آشنا کنیم. طیف سنجی NMR به ویژه 13CNMRو 1HNMR به صورت بسیار گستردهای در زمینههای مختلف شیمی، زیست شناسی، داروسازی، پزشکی، پتروشیمی و … دارد و به منظور کنترل کیفی، اطمینان از خلوص مواد و شناسایی ساختار ترکیبات مجهول مورد استفاده قرار میگیرد. امیدوارم که از مطالعه این مقاله لذت برده باشید. لطفا سوالات و نظرات خود را با ما در میان بگذارید.
مراجع
- Friebolin H & Becconsall JK. (2005). Basic one-and two-dimensional NMR spectroscopy (Vol. 7). Weinheim: Wiley-vch. 2005.
- Talsi, Evgenii, and Konstantin Bryliakov. Applications of EPR and NMR spectroscopy in homogeneous catalysis. Crc Press, 2017.
- Fan, Teresa W-M., and Andrew N. Lane. “Applications of NMR spectroscopy to systems biochemistry.” Progress in nuclear magnetic resonance spectroscopy 92 (2016): 18-53.
- Dolbier Jr, William R. Guide to fluorine NMR for organic chemists. John Wiley & Sons, 2016.
- Pretsch, Ernö, Thomas Clerc, Joseph Seibl, and Wilhelm Simon. Tables of spectral data for structure determination of organic compounds. Springer Science & Business Media, 2013.
- Scott, Robert A., and Charles M. Lukehart, eds. Applications of physical methods to inorganic and bioinorganic chemistry. John Wiley & Sons, 2013.
- Gonnella, Nina C. LC-NMR: Expanding the limits of structure elucidation. CRC Press, 2020.
- Hore PJ. Nuclear magnetic resonance. USA: Oxford University Press. 2015.
- Derome AE. Modern NMR techniques for chemistry research. Elsevier. 2013.
- Jacobsen NE. NMR data interpretation explained: understanding 1D and 2D NMR spectra of organic compounds and natural products. John Wiley & Sons. 2016.
- Bible RH. Interpretation of NMR spectra: an empirical approach. Springer Science & Business Media. 2013.
- Wüthrich K. Protein structure determination in solution by NMR spectroscopy. 1990. J Biol Chem. 1990. 265(36): 22059-22062. doi: 10.1016/S0021-9258(18)45665-7
- Xu S. 1D and 2D NMR experiment methods. 2011. Available online. .
- Silverstein RM. Spectrometric identification of organic compounds. New York: Wiley. 1991.
- Balci M. Basic 1H-and 13C-NMR spectroscopy. Elsevier. 2005.
- Skoog DA, Holler FJ, and Crouch SR. Principles of instrumental analysis. Cengage learning, 2017.
- Brown SP & Emsley L. Solid-state NMR. In: Vo-Dinh, T. (Ed.). Handbook of spectroscopy. John Wiley & Sons. 2006.
ما داده های خام به دست آمده از آنالیزهای زیر را بررسی و تفسیر میکنیم:


برای تفسیر طیف NMR نیاز به کمک دارید؟
برای ثبت سفارش و یا دریافت مشاوره رایگان باما در ارتباط باشید
09398565101 (تماس در ساعات اداری، تلگرام یا واتساپ)



سلام خیلی عالی و درست طیف ها رو برام تفسیر کردن
همراه با اطلاعات جامع و توضیحات عالی ، با پشتیبانی عالی هر وقت سوالی برام پیش اومده با صبر و حوصله فراون برام توضیح دادن ، از همه نظر تایید میکنم بهترین هستن.
متشکرم بابت به اشتراک گذاری نظرتون. موفق باشید.
بسیار عالی ، دقیق، در کمترین زمان ، و با حوصله و با پشتیبانی عالی
من به شدت راضی بودم ممنون از خدماتتون
سلام. ممنون که دیدگاهتون رو به اشتراک گذاشتید. موفق باشید 🌺
واقعا تفسیر طیف های NMR و IR برای من عالی بود دقیق و با جزئیات کامل. ممنونم و امیدوارم موفق باشید
سلام. ممنونم که دیدگاهتون رو به اشتراک گذاشتید. موفق باشید 🌺
سلام از هر نظر واقعا کارتون عالی هست، تحلیل تست هارو بصورت دقیق و جامع انجام دادین و اینکه پشتیبانی و پاسخگویی عالی دارین انقدر از کارتون راضی بودم که شمارو به دوستامم معرفی کردم و اوناهم خیلی راضی بودن از کار شما، خیلی خوشحالم از اینکه با شما آشنا شدم.
سلام.ممنون بابت به اشتراک گذاری دیدگاهتان. موفق باشید 🙏🌺